Ngay từ ngày 24/08/2021, Cara Therapeutics và đối tác kinh doanh Vifor Pharma đã thông báo rằng thuốc chủ vận thụ thể opioid kappa đầu tiên của công ty là difelikefalin (KORSUVA™) đã được FDA chấp thuận để điều trị cho bệnh nhân mắc bệnh thận mạn tính (CKD) (ngứa trung bình/nặng dương tính với điều trị thẩm phân máu), dự kiến sẽ ra mắt vào quý 1 năm 2022. Cara và Vifor đã ký thỏa thuận cấp phép độc quyền để thương mại hóa KORSUVA™ tại Hoa Kỳ và đồng ý bán KORSUVA™ cho Fresenius Medical. Trong đó, Cara và Vifor mỗi bên được chia sẻ 60% và 40% lợi nhuận từ doanh thu bán hàng ngoài Fresenius Medical; mỗi bên được chia sẻ 50% lợi nhuận từ doanh thu bán hàng từ Fresenius Medical.
Ngứa liên quan đến bệnh thận mạn tính (CKD-aP) là tình trạng ngứa toàn thân xảy ra với tần suất và cường độ cao ở bệnh nhân CKD đang chạy thận nhân tạo. Ngứa xảy ra ở khoảng 60%-70% bệnh nhân đang chạy thận nhân tạo, trong đó 30%-40% có ngứa vừa/nặng, ảnh hưởng nghiêm trọng đến chất lượng cuộc sống (ví dụ, chất lượng giấc ngủ kém) và liên quan đến trầm cảm. Trước đây, chưa có phương pháp điều trị hiệu quả nào cho tình trạng ngứa liên quan đến bệnh thận mạn tính, và việc phê duyệt Difelikefalin giúp giải quyết khoảng trống lớn về nhu cầu y tế. Việc phê duyệt này dựa trên hai thử nghiệm lâm sàng Giai đoạn III quan trọng trong hồ sơ NDA: dữ liệu tích cực từ các thử nghiệm KALM-1 và KALM-2 tại Hoa Kỳ và trên toàn thế giới, cùng với dữ liệu hỗ trợ từ 32 nghiên cứu lâm sàng bổ sung, chứng minh rằng KORSUVA™ được dung nạp tốt.
Cách đây không lâu, tin vui đã đến từ nghiên cứu lâm sàng về difelikefalin tại Nhật Bản: Ngày 10 tháng 1 năm 2022, Cara thông báo rằng các đối tác Maruishi Pharma và Kissey Pharma đã xác nhận rằng thuốc tiêm difelikefalin được sử dụng tại Nhật Bản để điều trị ngứa ở bệnh nhân chạy thận nhân tạo. Các thử nghiệm lâm sàng giai đoạn III. Mục tiêu chính đã đạt được. 178 bệnh nhân đã được dùng difelikefalin hoặc giả dược trong 6 tuần và tham gia vào một nghiên cứu mở rộng nhãn mở kéo dài 52 tuần. Mục tiêu chính (thay đổi điểm số trên thang đánh giá mức độ ngứa) và mục tiêu phụ (thay đổi điểm số ngứa trên thang đánh giá mức độ nghiêm trọng Shiratori) đã được cải thiện đáng kể so với ban đầu ở nhóm difelikefalin so với nhóm giả dược và được dung nạp tốt.
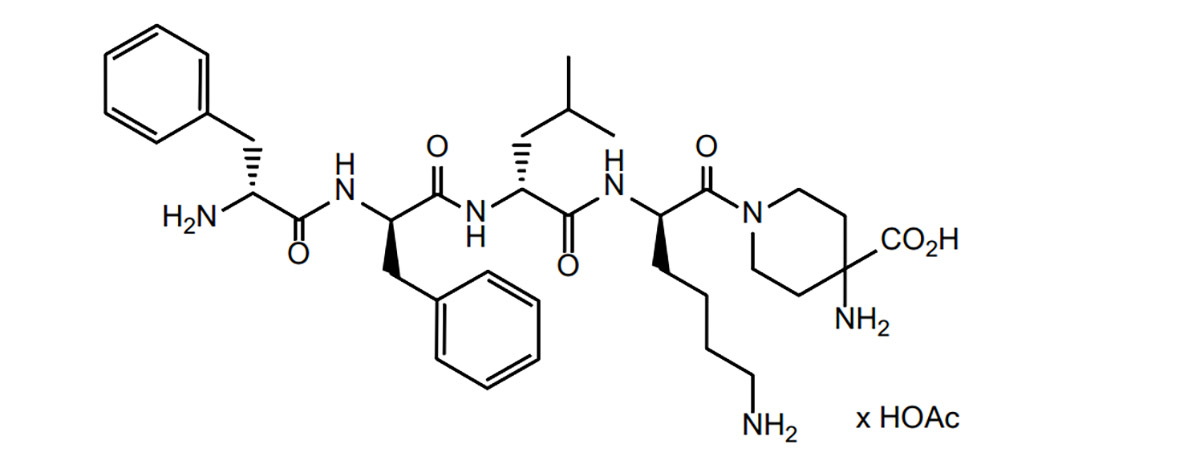
Difelikefalin là một nhóm peptide opioid. Dựa trên điều này, Viện Nghiên cứu Peptide đã nghiên cứu tài liệu về peptide opioid và tóm tắt những khó khăn, chiến lược phát triển thuốc peptide opioid, cũng như tình hình phát triển thuốc hiện nay.
Thời gian đăng: 17-02-2022