Chỉ định (sử dụng được chấp thuận): Năm 2019, FDA đã chấp thuận thuốc này để điều trị chứng rối loạn ham muốn tình dục giảm hoạt động (HSDD) mắc phải, tổng quát ở phụ nữ tiền mãn kinh khi tình trạng này gây ra sự đau khổ rõ rệt và không phải do các tình trạng y tế/tâm thần khác hoặc tác dụng phụ của thuốc.
Cơ chế hoạt động
PT-141 là chất chủ vận thụ thể melanocortin (chủ yếu là thụ thể MC4) có tác dụng điều chỉnh ham muốn tình dục thông qua các con đường của hệ thần kinh trung ương.
Không giống như chất ức chế PDE5 (ví dụ: sildenafil), chủ yếu ảnh hưởng đến mạch máu, PT-141 hoạt động tập trung để tác động đến ham muốn và sự kích thích tình dục.
Dược lý & Liều dùng
Cách dùng: Tiêm dưới da khi cần thiết (theo yêu cầu).
Liều dùng được chấp thuận: 1,75 mg tiêm dưới da
Dược động học:
Tmax ≈ ~60 phút
t½ ≈ 2–3 giờ
Tác dụng có thể kéo dài vài giờ, một số báo cáo cho biết có thể lên tới ~16 giờ.
Hiệu quả lâm sàng (Thử nghiệm giai đoạn III – RECONNECT, 24 tuần, RCT)
Điểm cuối chính:
Chỉ số chức năng tình dục nữ – Lĩnh vực ham muốn (FSFI-D)
Thang đo mức độ đau khổ tình dục ở phụ nữ (FSDS-DAO)
Kết quả chính (nghiên cứu gộp 301 + 302):
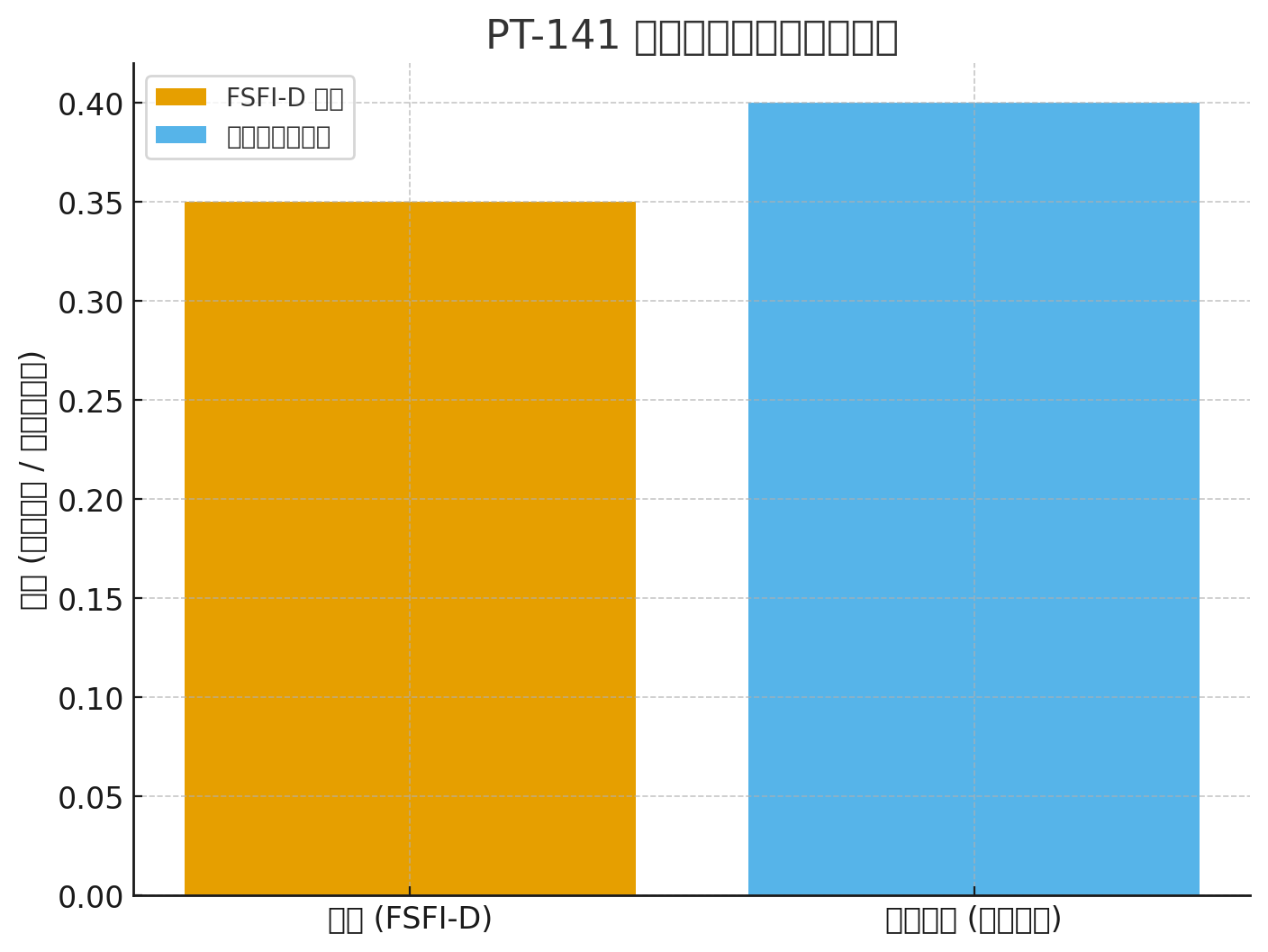
Cải thiện FSFI-D: +0,35 so với giả dược (P <0,001)
Giảm điểm FSDS-DAO: −0,33 so với giả dược (P <0,001)
Các điểm cuối khác: Các kết quả hỗ trợ (điểm chức năng tình dục, mức độ hài lòng do bệnh nhân báo cáo) có xu hướng tích cực, nhưng các sự kiện tình dục (SSE) thỏa đáng không phải lúc nào cũng cho thấy sự khác biệt đáng kể nhất quán.
Các sự kiện bất lợi (thường được báo cáo nhất trong các thử nghiệm)
Phổ biến (≥10%):
Buồn nôn (~30–40%; lên đến ~40% được báo cáo trong các thử nghiệm)
Xả nước (≥10%)
Đau đầu (≥10%)
Tác dụng lên tim mạch:
Người ta quan sát thấy huyết áp tăng tạm thời và nhịp tim thay đổi, thường sẽ hết trong vòng vài giờ.
Chống chỉ định hoặc thận trọng khi sử dụng cho bệnh nhân tăng huyết áp không kiểm soát được hoặc bệnh tim mạch.
Gan: Có báo cáo hiếm gặp về tình trạng tăng men gan thoáng qua; các báo cáo trường hợp cực kỳ hiếm gặp cho thấy có thể bị tổn thương gan cấp tính, nhưng không phổ biến.
An toàn dài hạn (Nghiên cứu mở rộng)
Một nghiên cứu mở rộng nhãn hiệu trong 52 tuần đã phát hiện ra sự cải thiện bền vững về ham muốn mà không có tín hiệu an toàn lớn nào mới.
Hồ sơ an toàn lâu dài được coi là dung nạp tốt, với các vấn đề chính về khả năng dung nạp vẫn là các tác dụng phụ ngắn hạn như buồn nôn.
Ghi chú sử dụng chính
Đối tượng được chấp thuận có hạn: Chỉ dành cho phụ nữ tiền mãn kinh mắc bệnh HSDD toàn thân mắc phải.
Chưa được chấp thuận rộng rãi cho nam giới (rối loạn cương dương hoặc ham muốn thấp ở nam giới vẫn đang được nghiên cứu).
Việc sàng lọc an toàn là rất quan trọng: Cần đánh giá tiền sử tăng huyết áp, bệnh tim mạch và gan trước khi kê đơn.
Tóm tắt dữ liệu nhanh
FDA chấp thuận: 2019 (Vyleesi).
Liều dùng: Tiêm dưới da 1,75 mg, theo nhu cầu.
PK: Tmax ~60 phút; t½ 2–3 giờ; tác dụng lên đến ~16 giờ.
Hiệu quả (Giai đoạn III, gộp lại):
FSFI-D: +0,35 (P<.001)
FSDS-DAO: −0,33 (P<.001)
Các tác dụng phụ:
Buồn nôn: lên đến ~40%
Xả nước: ≥10%
Đau đầu: ≥10%
Tăng huyết áp tạm thời được ghi nhận.
Bảng so sánh & Biểu đồ (Tóm tắt)
| Nghiên cứu / Kiểu dữ liệu | Điểm cuối / Đo lường | Giá trị / Mô tả |
|---|---|---|
| Giai đoạn III (301+302 gộp lại) | FSFI-D (miền mong muốn) | +0,35 so với giả dược (P <0,001); FSDS-DAO −0,33 |
| Sự kiện bất lợi | Buồn nôn, đỏ bừng mặt, đau đầu | Buồn nôn ~30–40% (tối đa ~40%); đỏ bừng mặt ≥10%; đau đầu ≥10% |
Thời gian đăng: 30-09-2025